近日,北京化工大学材料科学与工程学院徐福建教授团队和济宁医学院的李敬博士在Adv. Mater.上发表了题为“Flexible Modulation of Cellular Activities with Cationic Photosensitizers: Insights of Alkyl Chain Length on Reactive Oxygen Species Antimicrobial Mechanisms”的研究论文。

阳离子光敏剂与带负电荷的细菌和真菌具有良好的结合能力,在抗菌光动力疗法(aPDT)中应用广泛。然而,阳离子光敏剂对病原菌,尤其是真菌与哺乳动物细胞不具有选择性,往往会存在生物安全性的问题。同时,由于缺乏对相同光敏剂的系统性研究,目前尚不清楚细菌的哪些生物活性分子位点是光动力的有效损伤位点。因此,以小檗碱(BBR)为光敏剂核心,设计并合成了一系列具有不同烷基链长度的阳离子聚集诱导发光(AIE)衍生物(CABs),用于灵活调节阳离子光敏剂对细胞活性物质的选择性。BBR核心可以有效地产生活性氧(ROS),并在生理环境中实现高性能的aPDT。通过精确调节烷基链长度,实现了CABs在细菌、真菌和哺乳动物细胞中的不同结合、定位和光动力杀伤效果。研究发现,aPDT更有效的损伤位点是细胞内活性物质(DNA和蛋白质),而不是细菌膜。中等长度烷基链的CABs在光照下能有效地杀死革兰氏阴性菌和真菌,同时仍然保持良好的生物安全性。
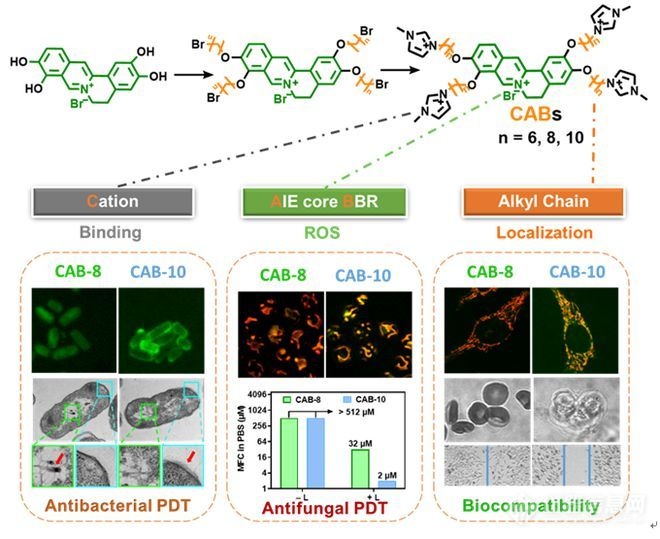
通过HOMO-LUMO实验证明烷基链长度的改变并不会改变核心BBR的AIE性能,但是随着烷基链的增长,CABs更容易形成分子间聚集体。与此同时,随着烷基链的增长,CABs与细菌的结合速率与结合量增加。CAB-8光照时的抗菌性能提升更明显。进一步的激光共聚焦定位实验证明,烷基链长调控CABs在细菌内的定位,CAB-8进入细菌,CAB-10卡在膜上。通过分子动力学模拟实验发现,CAB-10比CAB-8要克服更大的自由能,导致CAB-10卡在细菌膜上。透射电镜冷冻切片证明,CABs的定位调控杀伤,CAB-8损伤菌内活性物质,CAB-10损伤细菌膜上。进一步通过液质联用、DNA彗星实验以及β-半乳糖苷酶检测证明:CAB-10(膜上)膜损伤程度大于CAB-8(膜内),CAB-8(膜内)对DNA、酶损伤程度大于CAB-10(膜上)。随着烷基链的增加,CABs进入真菌的能力增强:CAB-10>CAB-8 >> CAB-6。同时,烷基链越长,CABs进入哺乳动物细胞的能力越强,具体表现为CAB-10的细胞毒性远大于CAB-8和CAB-6。综上所述,CAB-8可以很好的平衡光动力杀菌和生物相容性,具有高效杀菌性和生物安全性。该研究通过烷基链的定位调控,解决了阳离子光动力抗菌材料对细菌、真菌、哺乳动物细胞不具有选择性造成的生物安全问题,同时证明了相对于细菌膜来说,细菌内部的活性物质是光动力更为有效的氧化位点。本研究有望为构建具有良好选择性的高性能阳离子光敏剂提供系统的理论和研究指导。
北京化工大学材料科学与工程学院博士生郑良和博士生朱艺文为本文的共同第一作者。材料科学与工程学院徐福建教授和俞丙然教授、济宁医学院的李敬博士为本文的通讯作者。北京化工大学为第一完成单位。本研究工作得到了国家重点研发计划,国家自然科学基金,和北京市优秀青年科技人才计划的资助。
