本文来自微信公众号:iSynBio造物 (ID:gh_1c7f920d8f21),作者:未央,编辑:杳心,原文标题:《生命的起源:从RNA假说到多肽假说的争鸣?》,题图来自:视觉中国
科学家在关于地球生命起源的推测中,通常更加支持“RNA世界”假说(在DNA及其编码的蛋白质进化之前,第一个生物体是基于RNA链的),“蛋白质世界”假说的地位往往排在“RNA世界”之后。然而,一个新的计算模型阐述了早期蛋白质在足够长的时间如何折叠成有用的形状的过程。如果这个模型被验证为正确的话,那么这可能会恢复蛋白质作为生物起源分子的声誉。
如果不是RNA世界呢?
对于研究生命起源的科学家来说,困扰他们的最大的问题之一:先有蛋白质还是核酸(DNA和RNA)?大约40亿年前,基本的化学构件产生了更长的聚合物,这些聚合物具有自我复制和执行生命必需功能的能力:即存储信息和催化化学反应。
在生命史的大部分时间里,核酸负责前者的工作,蛋白质负责后者的工作。DNA和RNA带有制造蛋白质的指令,而蛋白质将这些指令提取并产生DNA或RNA。如果时间回溯到生命起源之初,这两种分子究竟哪个可以独自处理这两项工作?
几十年来,这个问题的答案的最受欢迎的候选者一直是RNA——特别是自1986年发现RNA也可以像蛋白质一样折叠和催化反应以来(1986年,Walter Gilbert发现多种RNA核酶具有催化活性)。
后来越来越多的理论和实验证据进一步支持了“RNA 世界”假说,即“生命从RNA中出现,可以催化更多RNA的形成”。在“RNA世界”里,生命可能以复杂的原始RNA链形式存在,它们既能复制自己,又能催化化学反应发生。后来,这些“RNA酶”可能进化出了制造蛋白质的能力,并最终将它们的遗传信息转化为更稳定的DNA。
但RNA非常复杂和敏感,一些专家怀疑它是否会在生命起源前世界的严酷条件下自发产生。此外,RNA分子和蛋白质都必须采用长折叠链的形式才能发挥催化作用,而早期的恶劣环境似乎会阻止核酸或氨基酸串变长。
纽约石溪大学的Ken Dill和Elizaveta Guseva以及加利福尼亚州劳伦斯伯克利国家实验室的Ronald Zuckermann在美国国家科学院院刊(PNAS)上提出了一个可能的模型来解决这个难题(https://doi.org/10.1073/pnas.1620179114)。
他们的模型起初非常简单——Dill在1985年开发它以解决蛋白质折叠问题,他将这个模型称之为“HP晶格模型”。“HP晶格模型”把20种常见蛋白质氨基酸分为两类:疏水型氨基酸(H)和亲水型氨基酸(P)。
Dill将其比作项链上不同颜色的珠子:蓝色的亲水珠(极性单体)和红色的疏水珠(非极性单体)。“珠子链(蛋白质肽链)”上的“珠子(氨基酸)”沿着二维格子的顶点按顺序发生折叠,就像将它们放在棋盘上一样。给定的珠子最终占据哪个方格取决于红色疏水珠子聚集在一起的趋势,这样可以使他们更好地避开水(见图2)。
图1 | 石溪大学的生物物理学家 Ken Dill 几十年来一直在研究蛋白质折叠。他现在正在利用这项工作来研究 40 亿年前发生的化学到生物学的转变
自催化折纸
生物物理学家Dill在整个1990年代使用这种模型来回答有关蛋白质序列和折叠状态的问题。直到最近,他才想到将该模型应用于早期地球生命起源前的化学向生物学的过渡。化学不是自私的,但基因是自私的,或者说,生命是自私的。“非自私”的化学是怎么变成“自私”的生物学的?这种“自私”诞生的第一颗种子是什么?这是Dill现在想解决的问题。
Dill认为,答案在于可折叠聚合物,也就是说在他眼中,像蛋白质这种由疏水或者亲水单体(即氨基酸)组成的,具有可折叠的二级甚至更高级结构的大分子聚合物,可能是生命的第一颗火种,而不是RNA。通过他的模型,他生成了一组疏水单体和极性单体的序列:所有可能的红蓝珠子项链的完整序列,这些序列最长可达25颗珠子。这些序列中只有2.3%折叠成紧凑的折叠结构,其中只有12.7%(仅占全部序列的0.3%)可以折叠成在其表面暴露出红色珠子疏水单体的构象。
这种表面暴露出疏水基团的构象可以作为漂浮序列的疏水部分的粘性着陆垫。如果单个红色珠子和红色尾链同时落在这个疏水性着陆垫上,从热力学角度来看,这两个序列有很大的可能会自发连接在一起。换句话说,这种构象可以充当延长聚合物的催化剂,将这些反应加速十倍。Dill说,尽管速率提高有限,但意义却十分重大。
这是因为,大多数细长的聚合物只有小部分最终会发生折叠。当这种情况发生时,带有着陆垫的折叠分子不仅会继续形成越来越多的长聚合物,它们最终甚至还会构成所谓的自催化组——直接折叠分子或间接催化自身的形成。有时,两个或多个折叠分子可以通过相互催化来增强自身的催化反应。虽然这样的组合很少见,但一旦发生,这些分子的数量会呈指数增长。“这就像只需要点燃一根火柴,就可以引发一场森林大火。”Dill说。
“这就是这个自催化折纸的全部魔力”,Dill补充说,“一个小事件能够利用自身来影响更大的事件。”
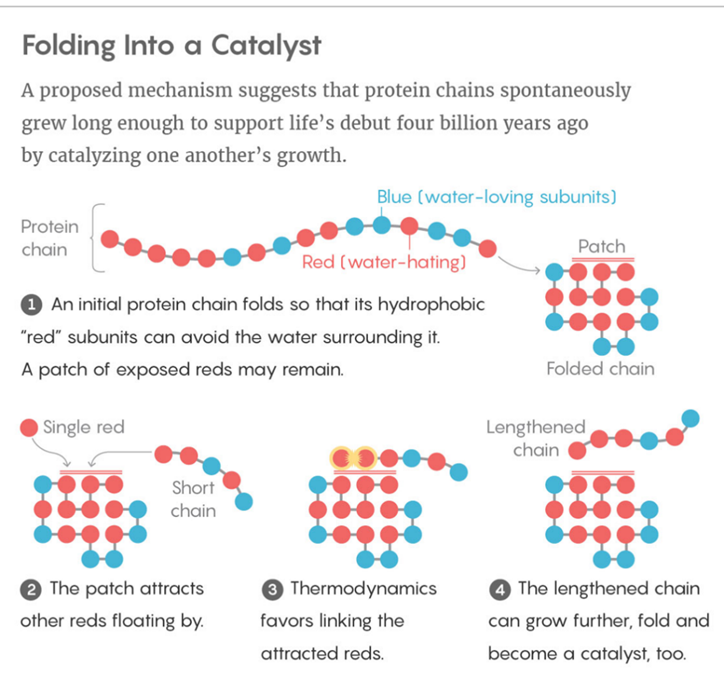
图2 | Ken Dill提出的HP晶格模型把蛋白质链上20多种氨基酸用小球表示,根据极性分为两种:亲水基和疏水基,分别用P(图示中的蓝球)和H(图示中的红球)表示。并规定每个氨基酸分子分布在二维或者三维格点上。对于一个合法的平面空间构型,用折叠形成的HH球相切数目的相反数(不包括蛋白质链上原有的HH球的邻接数)来表示构型的能量。能量越小的构型越接近自然构型,也就越可能存在。
“引发这一过程所需的是疏水性和极性基团的特定序列,你只需要这两个属性就可以通过他的模型预测出这个特定序列。”维也纳大学的理论化学家和名誉教授Peter Schuster说,“这是一个漂亮的理论结果。”
美国宇航局计算天体生物学和基础生物学中心主任Andrew Pohorille说:“这对基于RNA世界假说的生命起源的看法提出了质疑。对他和其他一些科学家来说,蛋白质似乎是一个‘更自然的起点’,因为它们比核酸更容易制造。”Pohorille认为,在生命最早的雏形中发现的信息存储系统可能不如目前细胞中基于核酸的系统先进。
“人们不喜欢蛋白质优先的假设,因为我们不知道如何复制蛋白质。”Pohorille补充道,“但这是一种尝试,表明即使你不能像复制RNA那样真正复制蛋白质,你仍然可以在没有那种精确信息存储的情况下建立和进化一个世界。”
“由于RNA在自催化方面的表现比蛋白质更好,因此从长远来看,它会更受到自然选择的青睐。但如果你从一个更简单的模型开始(比如Dill的),像RNA这样的东西可能会稍后出现,然后取代蛋白质成为生产游戏的赢家。”来自以色列魏茨曼科学研究所的基因组学研究员 Doron Lancet说。
寻找类肽的证据
当然,理论能否成功的关键还在于实际的实验。来自德国明斯特大学教授Erich Bornberg-Bauer说:“一切追溯到2.5到30亿年前的事情都是猜测。”如果该模型真的要与“RNA世界假说”进行一场斗争,它仍然需要在实验室中进行测试。否则,“这就像物理学家开的玩笑:假设奶牛是完全有弹性的球体。”德国马克斯普朗克发育生物学研究所的蛋白质进化系主任Andrei Lupas这样形容。同时他也认为RNA-肽世界,这两者能共同进化,“任何意义最终都需要有实证方法的支撑。”
这就是为什么Dill在PNAS论文上的合著者之一Zuckermann已经开始着手准备一个项目,他希望这个项目能够证实Dill的假设。
25年前,在Dill提出他的HP蛋白质折叠模型的时候,Zuckermann也开发了一种合成方法来制造被称为peptoids(类肽)的人造聚合物。他使用这些非生物分子来制造蛋白质模拟材料。现在,他正在通过类肽来检查序列如何折叠以及它们是否会成为良好的催化剂,以此来测试HP模型的准确性。Zuckermann说,在这个实验过程中,他和他的同事将测试数千个序列。
这个工作显然是混乱和困难的。因为Dill的HP蛋白质折叠模型高度简化,没有考虑现实情况中许多复杂的分子细节和化学相互作用。“这意味着我们将遇到模型无法看到的原子级现实。”Zuckermann说。

图3 劳伦斯伯克利国家实验室的化学家罗纳德·祖克曼(Ronald Zuckermann)拿着他使用称为peptoids(类肽)的人造聚合物形成的一种蛋白质样结构的模型。他现在正在使用拟肽来检验新的生命起源假说的预测。
至少目前,RNA世界假说仍占主导地位。尽管如此,Dill和Zuckermann对进一步研究的成果仍然持乐观态度。Dill计划使用该模型来研究有关生命起源的其他问题,包括遗传密码如何以及为何产生。Zuckermann希望这项研究——除了证实(或反驳)Dill 的计算——还将帮助他制造可用作药物输送载体、合成抗体或诊断工具的折叠体。
“这个模型为像我这样的实验者提供了一个起点”,Zuckermann说。“它提出了寻找这些原始催化剂的挑战,展示了它们是如何工作的,并说:这可能真的发生了。”
参考链接:https://www.quantamagazine.org/lifes-first-molecule-was-protein-not-rna-new-model-suggests-20171102/2).
本文来自微信公众号:iSynBio造物 (ID:gh_1c7f920d8f21),作者:未央,审核:懂个皮,编辑:杳心
